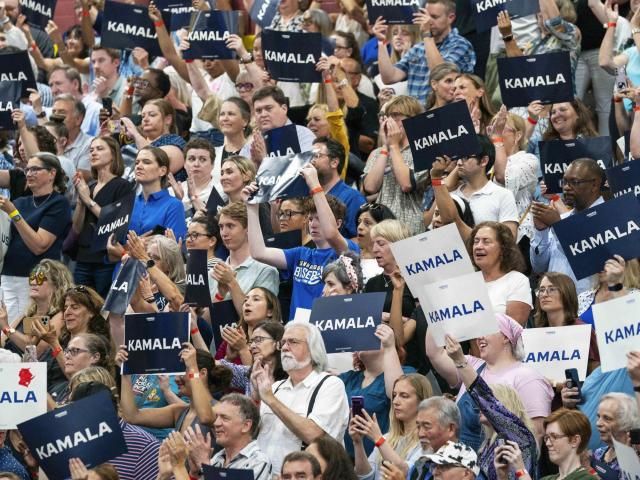为减少温室气体排放,需要从化石燃料向生物基碳氢化合物燃料过渡;然而,用于生物燃料生产的传统生物质种植与粮食生产竞争,并对生物多样性产生负面影响。最近,我们报道了一项两步光生物-光化学方法的原理验证研究,其中由光合蓝藻产生挥发性烃(异戊二烯),然后将其光化学二聚化成C10碳氢化合物。这两个步骤都可以利用太阳辐射。在这里,我们报道了一组更广泛的小1,3-二烯的三态(T1)敏化光二聚化,以确定哪些结构特征导致快速光二聚化。在365 nm辐照24 h后,1,3-环己二烯的收率最高(93%),其次是异戊二烯(66%)。1,3-环己二烯具有较长的三重态寿命,比非环二烯长两个数量级,这是其具有高光反应性的关键,也是源于其平面T1态结构。相比之下,异戊二烯构象柔韧,同时具有光化学和光生物学优势,因为它是挥发性1,3-二烯中反应性最强的,并且可以由蓝藻产生。最后,我们探讨了溶剂粘度、二烯浓度和三联体敏化剂负载对光二聚化的影响,重点关注了光生物产生二烯的条件。我们的发现对进一步发展两步光生物-光化学方法来生产煤油生物燃料是有用的。
小烯烃和共轭二烯是石油化工行业的重要组成部分。它们可以被寡聚成更大的烃链,从而生产出能量密度在C8-C16范围内的燃料,适用于航空燃料[1]。目前,小型共轭二烯主要是化石基石脑油蒸汽裂解生产乙烯的副产物[2,3]。因此,最近人们非常关注通过直接从生物体(如微生物、藻类和植物)以及从生物质衍生的糖和植物油中生产小生物基共轭二烯的更可持续的途径[4]。
微生物直接生物技术生产C8-C16烃是可能的[5,6,7,8];然而,由于这些碳氢化合物在细胞中积累并干扰细胞膜完整性的毒性,这一过程受到限制[9]。除此之外,大分子的提取和纯化过程需要能源密集型程序,导致生产成本增加。作为克服这些复杂问题的替代方法,我们最近提出了一种两步光生物-光化学方法,其中光合蓝藻直接从CO2、水和(太阳)光中产生挥发性异戊二烯,然后将其光化学二聚化成C10单萜[10]。第二步是三致敏光二聚化,也可以由太阳光运行。事实上,共轭二烯的三态光敏二聚化是有机光化学中产生[2 + 2]、[4 + 2]和[4 + 4]环加合物的既定方法[11,12,13,14,15],加氢后,环加合物作为具有高能量密度的煤油型燃料具有吸引力[16]。我们通过异戊二烯对生物喷气燃料进行光生物-光化学方法的生命周期评估表明,气候变化的影响约为化石喷气燃料的20%[10]。那么,这种方法是否也适用于,例如1,3-丁二烯?
第四代生物燃料的一般方法是利用转基因光合微生物直接从二氧化碳、水和阳光中生产有机化合物(图1),从而避免了生物质的种植、收获和加工[17,18]。据报道,最近蓝藻代谢工程的进展产生了短链烯烃[19,20],包括异戊二烯[21]。人们也可以通过更短的碳氢化合物,如光合作用产生的乙烯[19,22],形成共轭二烯,如2,4-己二烯[23]。此外,代谢工程的非光合微生物可以产生其他共轭二烯(如1,3-丁二烯)和三烯[24,25],将相应的基因纳入光合微生物可能是一种可行的途径。
图1

我们的光生物和光化学结合生产C8-C12碳氢化合物的原理,以及本工作所研究的方面。来源代表:光合微生物,木质纤维素(发酵)和植物油。详情见正文。PS=光敏剂,1,1-二萘基甲烷酮
虽然微生物直接光合作用生产1,3-二烯仍处于早期阶段,二烯的产量太低,无法大规模应用[21],但这些化合物也可以通过生物质加工生产(图1)。植物油衍生物和微藻脂已被用于一系列化学转化,包括齐聚化和烯烃复分解[26]。后者可作为常见副产物产生1,4-环己二烯[27,28],该化合物可通过光异构进一步转化为1,3-环己二烯[29,30,31]。除了生物生产1,3-环己二烯外,其他工业上重要的二烯也可以通过多种可再生方法生产,包括:(i)生物衍生乙醇、C4醇和二醇催化转化生产1,3-丁二烯[3,32];(ii)酸催化离子液体中蒎醇脱水生产2,3-二甲基-1,3-丁二烯[33];(iii)木质纤维素生物质生产1,3-戊二烯[34,35]。虽然一些研究集中在从生物质糖发酵生产二烯上,但没有一种途径已经商业化用于工业生产。
综上所述,几种(照片)生物方法正在开发用于共轭二烯的生产。同样,小碳氢化合物转化为燃料的几种方法也存在,从传统的和商业上建立的C-C键形成反应,如费托合成和酸催化寡聚化[36,37],到最近发展的热反应和/或金属催化反应[38,39]。从可持续发展的角度来看,需要进一步开发小碳氢化合物低聚化的途径,以减少对环境的影响。在这里,可见光或近紫外光引发的光化学寡聚化反应对这类途径的发展具有重要意义,因为这些反应可以利用太阳光作为主要的能量来源。在这种情况下,我们最近发现,具有共轭二烯单元的单萜类和倍半萜类可以在太阳光下光二聚成可作为生物柴油和润滑油的产品[40]。因此,尽管小而易挥发的1,3-二烯可以特别适合利用光合微生物进行生物技术生产。小共轭二烯的可再生来源也多种多样。结合它们的阳光驱动的光二聚化作用,这可以成为减少航空燃料生产对环境影响的一条途径。
为了指导未来的光生物学工作,我们现在寻求找出哪些共轭二烯最容易光化学转化为二聚体,并提出以下问题:取代基和1,3-二烯的结构如何影响光化学二聚化?影响三致光二聚化的主要因素是什么?另一种比异戊二烯更小的共轭二烯能提供更有效的光二聚化吗?我们使用1,1-二萘基甲烷作为光敏剂(PS,图1),因为它已被确定为太阳照射下的合适光敏剂[10,40,41]。研究了溶剂粘度、稀释度和光敏剂负载对二聚化收率的影响,并考虑了光生物二烯生产的相关条件,对这些因素进行了优化。我们的工作可以为未来的光生物-光化学联合生产煤油型生物燃料提供有益的见解。
异戊二烯(质量纯度> 99%)、2,3-二甲基-1,3-丁二烯(98%)、e -1,3-戊二烯(90%)、2,4-己二烯(90%)、1,3-丁二烯(15wt . %)、3-甲基-1,3-戊二烯(98%)、1,3-环己二烯(97%)、1,3-环庚二烯(95%)和Z,Z-1,3- 1,3-环二烯(97%)从Sigma-Aldrich中得到。除另有说明外,所有化学品均直接使用。在光化学反应之前,从下列二烯中去除叔丁基儿茶酚:异戊二烯、2,3-二甲基-1,3-丁二烯和1,3-环己二烯。根据文献报道合成1,1-二萘基甲烷酮。[10]值得注意的是,1,3-丁二烯的己烷溶液不含任何稳定剂。
将一种无抑制剂(叔丁基儿茶酚)的液态二烯与1,1-二萘基甲烷(光敏剂用量为0.1-0.5 mol%)混合。本研究中使用了两种不同体积的反应溶液:在所有实验中使用5 mL的纯二烯(> 90 wt%);稀释二烯(< 60% wt%)反应用20ml。然后使用冷冻泵-解冻循环(3次)将二烯和光敏剂的溶液脱气,并留在氩气气氛中。然后使用注射器将均质溶液转移到盘管反应器(特氟龙管od值× id): 3.18 mm × 2.1 mm,环路尺寸~ 20ml)[10]用隔片密封。反应器先前用氩气吹扫3分钟。然后将盘管式反应器在恒温(7°C)下连接到冷水机,以保持反应在低温下,以避免压力积聚或起始材料的损失。RPR-100或-200 Rayonet光化学室反应器用于光反应。光化学反应在365 nm(氙灯,16 × 24 WUV灯,购自Southern New England Ultraviolet Company)照射下启动,持续24小时(如未注明)。通过便携式辐射计(从Opsytec购买的RM12光谱辐射计)测量,反应器中的光强度约为8 mW/cm2(如果没有另行说明)。反应时间结束后,溶液以戊烷为洗脱液通过硅胶柱。用减压蒸馏法分离了二烯二聚体。
采用Agilent 7890A GC - 5975 MSD系统监测光化学反应,采用分次进样(进样量为1 μL;分割比例:100:1;进口温度250℃;流速:120 mL/min)和毛细管柱(19091S-433: 325℃:30 m × 250 μm × 0.25 μm)(前SS入口:He;:真空))。柱箱的初始温度为70℃(0.5 min平衡时间),样品运行的最终温度为320℃。温度速率设置为20°C/min,总运行时间为12.5 min。载气为氦气,流速为1.2 mL/min。质谱仪的源温和源温分别为230℃和150℃。用重量法测定了二聚体的总收率。1H NMR谱在JEOL (400YH磁体)共振400 MHz光谱仪上记录。化学位移δ以ppm为单位,耦合常数J以Hz为单位。1H NMR化学位移参考残余溶剂信号(CDCl3, 1H 7.26 ppm)。
几何优化采用Gaussian16在(U)B3LYP-D3/6-311 + G(d,p)水平进行[42,43,44,45]。用不受限制的Kohn-Sham DFT形式计算了三重态。通过频率计算,将平稳点表征为最小或过渡状态。力学研究中使用的吉布斯自由能是在298 K时计算的。
摘要
1 介绍
2 实验
3.结果与讨论
4 结论
数据可用性
参考文献
致谢
作者信息
道德声明
补充信息
搜索
导航
#####
在分析环1,3-二烯之前,我们的分析首先从实验和计算相结合的方式探索结构对非环1,3-二烯光二聚化的影响。随后,我们探讨了异戊二烯稀溶液的光二聚化反应以及三联体增感剂负载和溶剂粘度的影响。
我们选择了一系列不同的1,3-二烯(1 - 9,图2)来研究分子结构对光敏二聚化的影响。我们首先关注的是1-7。这组化合物允许我们探索(i)增加甲基取代基的数量,(ii)甲基取代基在共轭二烯上的位置,即在中心C2/C3原子取代与末端C1/C4原子取代,以及(iii)无环与环结构的影响。并不是所有的二烯1 - 7都是挥发性的,但我们可以用这些来评估对1,3-二烯三致敏光二聚化的结构影响。值得注意的是,有第四个二甲基-1,3-丁二烯异构体,2-甲基-1,3-戊二烯;然而,它不容易获得,沸点为78°C。因此它被排除在外。在后面的章节中,我们将讨论T1状态下较大的环烷-1,3-二烯8和9,以探讨环尺寸对二烯片段扭曲的影响及其对二烯二聚化收率的影响(见下文)。我们没有考虑小的1,3-环戊二烯,因为它通过Diels-Alder反应在几个小时内热二聚。
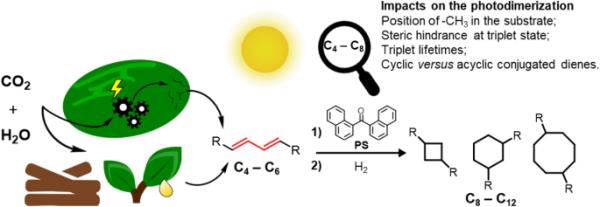
图2
本研究研究的1,3-二烯及其沸点(b.p): 1,3-丁二烯1,异戊二烯2,2,3 -二甲基-1,3-丁二烯3,e -1,3-戊二烯4,2,4-己二烯5,3-甲基-1,3-戊二烯6,1,3-环己二烯7,1,3-环七烯8,Z,Z-1,3-环己二烯9
表1列出了共轭二烯1- 7和光敏剂1,1-二萘基甲烷在(U)B3LYP-D3/6-311 + G(d,p)水平上的三重态能E(T1)。由于我们在5和6的实验中使用了Z-和E-异构体的混合物,我们计算了所有异构体的E(T1)。1,1-二萘基甲烷酮(52.2 kcal mol?1)的E(T1)略高于本文所研究的二烯类,是我们研究中比较合适的增敏剂。1,1-二萘基甲烷的三重态寿命为300 ns[41],足以发生分子碰撞和能量转移。此外,1,1-二萘基甲烷的T1态具有ππ*特征,这阻止了竞争性的h原子抽离途径[46]。
表1小的1,3-二烯的三重态能和光二聚化产率(0.1 mol% 1,1-二萘甲烷),除非另有说明,使用纯二烯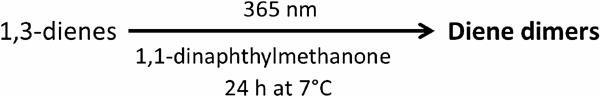
所有的二聚化反应都在环绕水冷冷凝器的聚四氟乙烯管中进行(图3),使用纯二烯,除了1,3-丁二烯(1),它在己烷中稀释,即在商业上可用的形式。以0.1 mol%的光敏剂负载对二烯2-7进行光照射(λ=365 nm, t=24 h)得到的二聚体产率如表1所示。考虑到光敏剂1,1-二萘基甲烷在整个研究中都是保留的,从应用的角度来看,我们的比较基于二聚体产物的产率而不是量子产率。
图3

水冷式冷凝器周围的聚四氟乙烯盘管用于二烯的光二聚化反应。反应在~ 7℃下进行。将含有二烯和1,1-二萘甲烷混合物的起始实验溶液转移到聚四氟乙烯管中,两端用橡胶隔条密封
所有辐照样品均可通过气相色谱-质谱分析证实二聚体的形成(图2)。S1-S3,应急服务国际公司)。在7和2中发现了微量的三聚体(图S4, ESI),并且光敏剂被保存在辐照样品中,没有形成h原子萃取产物(即二萘-1-基)甲醇,图S5, ESI)。有趣的是,在色谱图中观察到光二聚化的不同程度的选择性,因为一些二烯比其他二聚体产生更多的不同的二聚体异构体(图2)。S1-S3,应急服务国际公司)。在5的情况下,产品中大量的二聚异构体可以追溯到原料中不同的异构体。考虑到我们对二聚体的总产率感兴趣,我们不评估每一种二聚体的具体结构。早期的研究对一些1,3-二烯的二聚体结构进行了详细的探索,发现异戊二烯、1,3-环己二烯和2,3-二甲基-1,3-丁二烯的光敏二聚反应分别为7、3和7种不同的二聚体[11,13]。这些产品混合物(二聚体异构体)的组成强烈依赖于所使用的光敏剂和在S0状态下可用的二烯构象之间的分布[11,13]。有趣的是,不同的1,3-二烯在二聚体的产率上有很大的差异,从93%到9%以下。在非环二烯(2 - 6)中,2的收率最高,3和4次之,5和6的收率最低(均为~ 9%)。在这一点上,可以注意到5也表现出低的敏化Z/ e光异构量子产率。[47]
1,3-丁二烯光二聚化反应只能在正己烷溶液中进行(市售为15%),并且观察到的产率仅为6.5%。现在,当2和5(分别是活性最强的无环二烯和活性最低的无环二烯)在与1相同的条件下在己烷中运行时,2的二聚体的产率仍然高于1(18%),而5的二聚体的产率则从9%下降到1%(表1,脚注e)。这些结果表明,5的活性远远低于1,并且与6一起是活性最低的无环1,3-二烯。由于在我们选择的小的无环1,3-二烯中,2的产率仍然是最高的,从光化学的角度来看,2显然比1有优势,而且它已经可以光生物学地产生。1的一个潜在好处是,它应该比2更容易从细胞中蒸发。
接下来,我们使用DFT计算来确定所研究的1,3-二烯之间不同反应性的原因。共轭二烯光敏二聚化的反应机理可以看作是三个主要步骤的序列,如方案1所示:(i)光敏剂激发到三重态;(二)能量转移和(三)二聚化。我们研究了甲基取代对共轭二烯的E(T1)和生成二聚自由基对中间体(方案1中步骤iii的第一个产物)的步骤的活化能和反应能的影响。
方案1
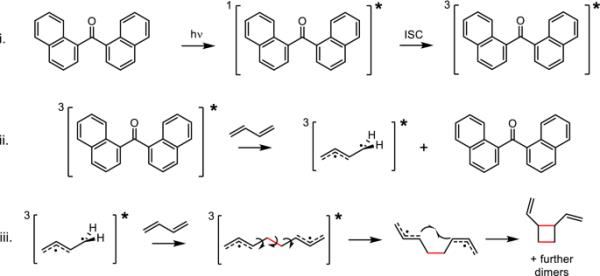
共轭二烯光敏二聚化反应机理的三个主要步骤:(1)光敏剂(1,1-二萘基甲烷)激发为三重态;(ii)从光敏剂到基态二烯的能量转移;(iii)二聚化步骤,由T1二烯向50二烯的攻击开始,导致双(烯丙基)自由基对中间体环化后产生环状产物,这里以最简单的二烯1,3-丁二烯为例。所示的产物只是可能的二聚体中的一种(4-、6-和8-元环,取决于最后一步中的自由基组合)。反应中形成的化学键用红色表示。ISC系统间交叉
在T1状态下,无环共轭二烯可以描述为由两个相互不相互作用的自由基垂直取向组成的三重态自由基对;一个烷基自由基和一个烯丙基自由基(图4A和S6, ESI)。另一方面,第一步反应的产物可以被描述为具有三重态多重性的双(烯丙基)自由基对二聚体(图4B),这是一种短暂的中间体,它经历了系统间与单线态自由基对的交叉,然后与所观察到的二聚体闭合。然而,当它们处于单线态时,双(烯丙基)自由基对也可能在竞争性反应中,通过中心C-C键的断裂而解离,从而产生两个二烯反应物(见下文)。
图4
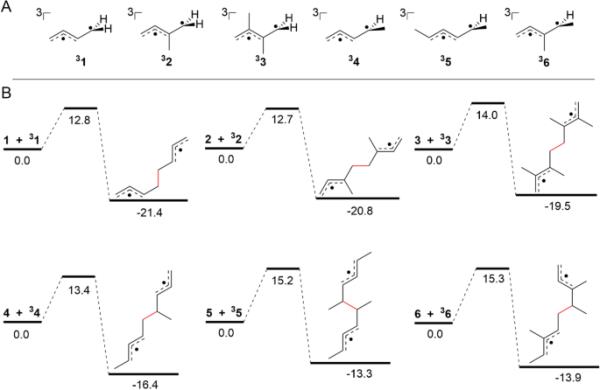
基于优化(U) B3LYP-D3/6-311 + G(d,p)几何结构的T1态二烯1-6最稳定构象示意图。在(U) b3lypp - d3 /6 - 311 + G(d,p)的水平上,以298 K的吉布斯自由能计算得到T1二烯与S0二烯生成双烯丙基自由基对中间体的活化能(kcal mol?1)。所选择的T1二烯和S0二烯的构象是最稳定的构象,它们结合在一起在过渡态产生最小的位阻,并且可能具有最低的激活势垒
甲基取代基具有两种作用:它们对T1态二烯中形成的烷基和烯丙基自由基具有超共轭稳定作用;然而,甲基取代基越多,导致二聚基对中间体的过渡态空间拥塞就越广泛。对于三态二烯和二聚基对中间体在其最不拥挤(最稳定)的构象,甲基取代基只提供超共轭稳定。另一方面,空间效应在过渡态起作用。前三个无环二烯(1-3)采用最低能量构象,描述为一个伯烷基自由基和一个烯丙基自由基,而4-6采用三态构象,描述为一个叔烷基自由基和一个烯丙基自由基。
那么为什么异戊二烯在无环二烯中产率最高呢?当第二个甲基连接到中心的2 - C原子上导致3时,以及当2 -甲基被移除导致1时,产率都会降低。首先,我们考虑1 - 3(分别为0.6、0.0和0.3 kcal mol - 1)的相对E(T1),这并不表明随着甲基取代的增加T1状态逐渐稳定。在32的最稳定的构象中,甲基位于烯丙基自由基的一端(在内端)。在33中,两个甲基都连着内部的C原子,其中一个甲基连着33烯丙基部分的C2原子。在这个位置,单占据分子轨道(SOMO)没有系数,与2相比,这个甲基没有提供额外的稳定性。我们还应该比较2和4这两个同分异构体,虽然4和2的E(T1)是相同的,但34最稳定的构象中的甲基位于烷基基部分,而32则必须位于烯丙基部分。最后,在二甲基取代的5和6上,我们可以注意到一些同分异构体的E(T1)降低了。然而,对于Z,Z-5和Z-6,这些应该源于不稳定的空间阻塞在50状态。然而,E-6的E(T1)也很低,低能量表明T1态的烷基和烯丙基自由基部分都具有超共轭稳定性。
三态猝灭速率常数在不同的二烯猝灭剂中有差异[48],Sandros和B?ckstr?m认为三态能量传递是一个扩散控制的过程[49]。光敏剂空间位阻的变化也被证明不会影响羰基化合物到不同底物的能量转移[50]。我们之前发现,速率决定步骤是将T1态二烯加入到50态二烯中,从而形成三联体双烯丙基自由基对中间体[10]。每个三联体1,3-二烯中最活泼的部分是烷基自由基部分。考虑到两种反应物的各种可能的构象,我们考虑了最稳定构象中的T1态二烯与最稳定构象中的S0态二烯的反应路径,并讨论了两种反应物之间空间拥塞最少的激活势垒最低的反应路径。在5和6的情况下,考虑的s态构象是E-和E,E-异构体中最稳定的构象。此外,2、4和6中的每一个都可能有两个正交扭曲的T1态结构,因为这些二烯可以围绕C1-C2或C3-C4键扭曲(图4)。
首先,对应的S0二烯加31和32的活化能比3-6的活化能低。对于4-6,反应性烷基自由基位点是一个次生自由基,这解释了这些二烯稍微高一些的活化障碍。另一方面,与2相比,3具有较高的活化能和较低的二聚化产率,可能是由于3在二聚化过渡态有较大的位阻。这可以在几个属性中看到。首先,处于3二聚化过渡态的反应物分子33比处于2二聚化过渡态的反应物分子32更扭曲(33和32的计算畸变能分别为3.1和1.7 kcal mol?1)。3的光二聚化过渡态表现出比2更短的C-C键形成距离(图5),同时在3的情况下,来自两个二烯烃的氢距离更远(图S7, ESI)。然而,我们在实验中观察到的1的反应性较低的原因尚不清楚,因为它的计算活化能与2相似。这可能是由于1,1-二萘基甲烷敏化剂与1的E(T1)的能量差略大于该敏化剂与2之间的能量差。此外,1的双(烯丙基)自由基对形成的键比2的长0.009 ?(图5)。在这里,有人可能会认为,键距离越长,越有利于C-C键的裂解,从而导致初始二烯反应物的生成。事实上,在1中比在2中更容易的键裂可以解释在1的反应中二聚体的产率比在2中低。事实上,除了6外,所有的无环二烯都显示出C-C键距离与二聚化产率之间的相关性(图S8, ESI),表明这种竞争反应发生了。
图5
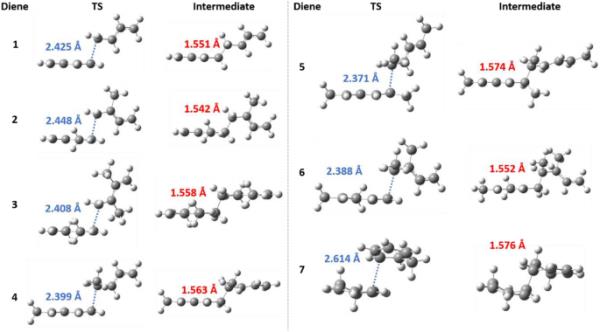
在(U)B3LYP-D3/6-311 + G(d,p)水平上计算了一个T1二烯与一个so0二烯加成时形成的过渡态(TS)和双烯丙基二聚体自由基对中间体的结构。表示了TS(蓝色)和中间体(红色)中形成键的键距
在同分异构体2和4中,二烯4在第一个二聚化步骤中的活化势垒比二烯4高0.7 kcal mol?1,这可能是由于反应的烷基自由基部分是34中的次级自由基。这解释了4的二聚化产率低于2的原因。
对于具有最稳定的仲烷基自由基构象的3种二烯4-6,存在具有伯烷基自由基构象的能量更高的构象。对于4,这种构象的相对能量比最稳定构象高0.7 kcal mol - 1,而对于6,这种构象的相对能量比最稳定构象高2.8 kcal mol - 1。在这个具有伯基位点的6的不太稳定的构象中,烯丙基自由基部分要么在相邻的两个C原子上的甲基取代基之间经历空间拥挤,要么采用甲基取代烯丙基自由基的不太有利的z构型。因此,在6的情况下,具有反应性伯烷基自由基基团的构象较少(图S9, ESI)。在二烯5中,甲基取代基位于二烯段的末端,因此,该二烯在T1态的烷基自由基部分始终是一个仲自由基部分。
当从1到5和6时,反应能逐渐减少,这部分可以用三联体二烯反应物的超共轭稳定性增加来描述。在31中,没有超共轭稳定,而在5和6中,三联体二烯经历烷基和烯丙基自由基部分的超共轭甲基稳定。因此,二聚化时的能量增益在后一种中较小。第二个影响因素可能是5和6的二聚化比1的二聚化熵损失更大,因为由于甲基取代基之间的空间冲突,两个第一二烯的产物在结构上更受限制。
1-6个速率决定步骤的活化能与反应能有一定的相关性(R2=0.80,图S10A, ESI),即加成步骤越快,激活势垒越低,符合Bell-Evans-Polanyi原理[51,52]。此外,在过渡态结构中计算的自旋密度显示了T1态和S0态反应双烯的明显区别(图S11, ESI),以及前者对后者的自旋极化效应。这些结果揭示了一个类似反应物的过渡态,与exergonic反应曲线一致(图4)。
值得注意的是,更取代的2,5-二甲基-2,4-己二烯,其T1态被描述为由叔烷基自由基和末端二甲基取代的烯丙基自由基组成,有报道称,当尝试敏化光二聚化时,不会形成二聚体[11]。这支持了我们观察到的1,3-二烯在这些光反应中的反应活性与烷基自由基部分C原子或其附近甲基取代的程度之间的关系。T1中的异戊二烯(2)是反应性最强的二烯,因为它是单甲基取代二烯,反应性烷基自由基部分是伯烷基自由基。它的异构体,胡椒烯(4),反应性较低,因为它在T1态的最稳定的构象具有仲烷基自由基部分。二甲基取代的二烯挥发性和/或具有活性较低的仲烷基基基团。
T1态7在共轭二烯段的两个末端C原子上具有显性自由基特征(图6A, B),该二烯在辐照24 h后二聚体的产率最高(93%)。12 h后二聚体的产率已达80 wt.%, 36 h后达到95 wt.%。显然,7具有无环1,3-二烯无法获得的特征,从而使动力学更快。
图6

环1,3-二烯7 - 9 T1态的几何形状(两个8构象)(U) B3LYP-D3/6-311 + G(d,p)水平,B它们的自旋密度(等值=0.004),C二面角(用红色和蓝色书写)。1,3-环庚二烯有两个最小值,它们的相对自由能用括号表示
事实上,7的光二聚化速度比2 - 6快得多(部分)应该是由于它的T1态寿命长1.3-6.0 μs[53],比2和5的分别为27和32 ns长两个数量级。[53]此外,由于平面T1态结构,37最好被描述为C1和C4上的两个局域自由基,由于平面π-轨道系统中两个相同自旋电子之间的泡利排斥而局域到这些原子上。因此,7的快速光二聚化有两个原因;(1)由于六元环的几何限制,它具有较长的三重态寿命[54],因此失活途径较少;(2)它的两个自由基相当地定位在1,4-二自由基中,因此具有较高的反应活性。具有更大和更灵活的环共轭二烯的T1寿命应该更短,8和9的T1寿命分别为400-550和40-120 ns[54,55]。从计算得到的环二烯7-9的T1态结构(图6C)来看,逐渐向无环二烯的结构转变变得清晰起来。
三联态环己二烯37具有C2对称,使得H-C1-C2-H和H-C3-C4-H的二面角均为9.3°。38可以存在于两种不同的构象中:最稳定的构象是端部H-C-C-H二面角均为6.5°的非扭曲c对称构象;第二种构象的相对能量为2.3 kcal/mol, H-C-C-H二面角为77.4°,有一个平面烯丙基自由基碎片。最后,39仅以一个烷基自由基和一个烯丙基自由基的扭曲构象存在,具有一个80.8°的H-C-C-H二面角。Allonas等人也发现了类似的结果[55],尽管他们的工作中没有注意到38(38 ')的扭曲构象。实际上,38 '可能是发生向S0衰变的构象。在39中,扭转水平与T1状态下的无环1,3-二烯相当(图S12, ESI),因此,其寿命与无环三联体二烯相似。随着环尺寸的增大,较短的三重态寿命和二烯两个末端C原子处的自旋密度逐渐降低(图6B),这将降低环1,3-二烯敏化光二聚化的效率。那么,这是如何反映在激活屏障上的呢?
如图7所示,随着环尺寸的增加,激活势垒变得更高,二聚化步骤变得更不符合人体。然而,7的第一个二聚化步骤的活化能甚至比1和2的活化能更低,这是由于非扭曲的37(一个平面1,4-二自由基)的反应活性更高,两个相同自旋电子之间存在泡利排斥。另一方面,与1和2的反应相比,7的反应不容易发生,这与在7的情况下形成更密集的二自由基中间体有关。此外,较长的T1寿命有助于7更快的二聚化,因为它导致37在T1状态下的浓度高于其他1,3-二烯。假设T1光敏剂与7之间的每次相遇都成功地进行了能量转移,并且这些相遇是扩散控制的(见ESI),我们估计T1态物质的浓度为:[37]=8.3 × 10-7 M, [38]=2.6 × 10-7 M, [39]=2.6 × 10-8和[32]=1.7 × 10-8 M(见ESI,第1.2节)。因此,37的浓度比两个较大的环二烯和异戊二烯的计算浓度高3到近50倍。
图7
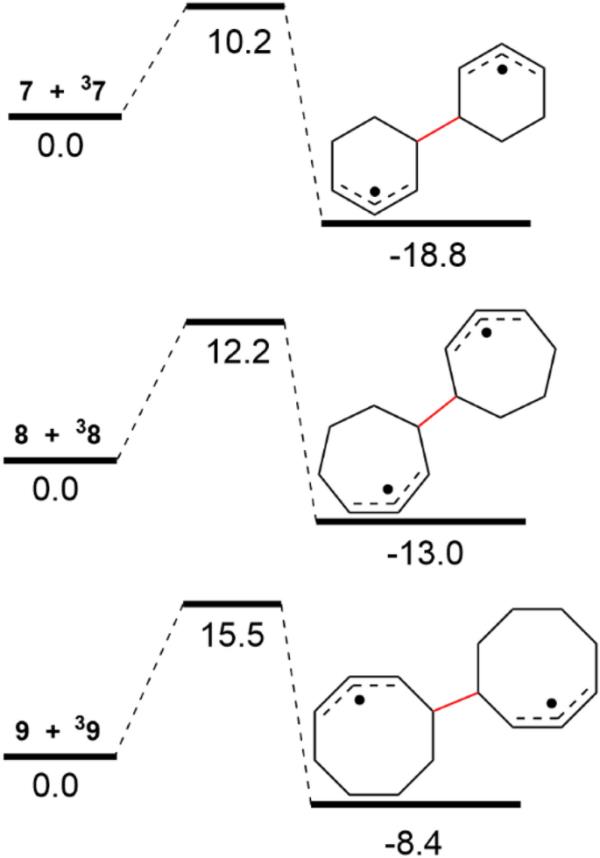
T1态二烯与50态二烯加成双(烯丙基)自由基对中间体的激活障碍,对于二烯7-9。在(U) b3lypp - d3 /6-311 + G(d,p)能级计算为298 K下的吉布斯自由能。生成的中间体的能垒和相对能均以kcal mol?1为单位,它们与反应物的能量有关
因此,我们在与7相同的条件下测试了较大的8和9的光敏二聚化,其产率分别为45%和7%(表1)。显然,随着T1状态下扭曲程度的增加,二聚体的产率降低,这证实了较大的环1,3-二烯在T1状态下的扭曲降低了光敏二聚化的效率。事实上,9的收益与5的收益相当。有趣的是,8的二聚体产率低于2,尽管其三态寿命明显更长(~ 500 vs. 27 ns)。值得注意的是,在8和9的反应中,观察到微量的分子内环化产物(图S13, ESI)。
综上所述,1,3-环己二烯和异戊二烯是光二聚化反应中最合适的底物。如果将1-9的第一个二聚化步骤的活化能与相应的反应能进行对比,可以看到7和8是异常值(图S10B, ESI)。包括7和8,线性回归的R2值为0.32,而没有这些化合物的值为0.79。二烯7和8的活化能比拟合预测的要低,这应该是由于它们的1,4-二自由基的局域性。
我们将进一步探索最佳反应条件。
在此之前,我们辐照了异戊二烯(15wt %)的己烷溶液,以便与1,3-丁二烯的相应结果进行比较。我们现在测试了不同浓度的异戊二烯溶液(5-60 wt%的己烷),保持恒定的光敏剂浓度(0.1 mol%),以探索稀释如何影响二聚化收率。低异戊二烯浓度是有趣的,因为它们类似于光生物产生的异戊二烯被捕获时产生的稀释溶液。如图8A所示,二聚体的产率随着异戊二烯浓度的降低而线性降低。
图8
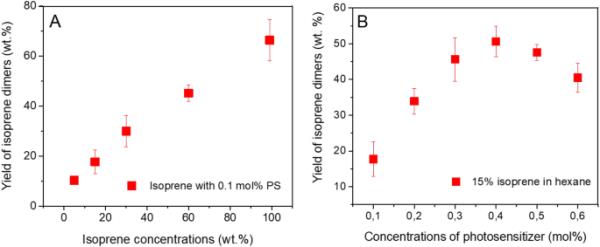
异戊二烯和1,1-二萘甲酮浓度对光二聚化收率的影响。A二聚体的总产率(wt%)与1,1-二萘基甲烷(0.1 mol%,与异戊二烯浓度有关)的异戊二烯浓度(5-99 wt%在己烷中)的函数。B 15%异戊二烯在己烷中光二聚化二聚体的总产率与1,1-二萘甲基甲烷浓度的函数关系(0.1-0.6 mol%)
我们还探讨了使用异戊二烯(15%的己烷)的己烷溶液增加光敏剂浓度(0.1-0.6 mol%)的影响。增加的敏化剂浓度应该有利于双分子三重态能量转移,如图8B所示,当添加0.4 mol%的1,1-二萘甲烷时,异戊二烯二聚体的产率增加了54%。这几乎是使用0.1 mol%光敏剂溶液的反应的三倍。然而,当使用0.5和0.6 mol%的光敏剂时,二聚体的产率下降,这是由于两个光敏剂分子之间的自猝灭或被一个光敏剂分子猝灭所致。虽然是内源性的,但由于异戊二烯的E(T1)接近敏化剂的E(T1),后者也可能发生[49]。因此,在己烷中异戊二烯浓度为15wt .%的稀释条件下,0.4 mol%的负载是光敏剂的最佳负载。我们还用更高浓度的光敏剂(0.4 mol%)测试了纯异戊二烯(99%),但在这种情况下,与0.1 mol%的情况相比,二聚体的产率没有增加(表S1, ESI)。因此,在异戊二烯浓度较低的情况下,增加光敏剂浓度可以提高光二聚化的效率,而在异戊二烯浓度较高的情况下则没有提高。
1,3-环己二烯在溶液中的光敏二聚化已被证明与粘度有关,二聚体的产率随着压力的增加而增加,因此,溶剂的粘度增加[56]。在低粘度范围内,从T1状态的衰变也依赖于溶剂粘度[57],表现为扩散限制过程。为此,我们测试了不同粘度的溶剂(己烷(0.3 cP)、环己烷(1.0 cP)、十四烷(2.3 cP)和十六烷(3.4 cP)),并在这些溶剂(15 wt%)和0.1 mol%的1,1-二甲基甲烷中对异戊二烯溶液进行了24 h的辐照实验。二聚体的相对产率通过1H NMR波谱(表2,图S14, ESI)评估,基于起始材料异戊二烯的质子整合与形成的二聚体质子的比率。
表2不同粘度的溶剂对异戊二烯(15wt %和0.1 mol% 1,1-二萘甲基甲烷)光二聚化的影响。样品辐照24h
与Liu等人[15]的早期观察结果相反,我们的结果表明,异戊二烯二聚体的产率确实受到溶剂粘度变化的影响;然而,在我们选择的范围内,粘度不是线性依赖的。事实上,从正己烷(0.3 cP)到环己烷(1.0 cP)和十四烷(2.3 cP),产率有所下降,但从十六烷(3.4 cP),产率又略有上升。就像T1衰变依赖于溶剂粘度一样,异戊二烯二聚体的产率仅在粘度值的低范围内依赖于粘度。在本文所研究的溶剂中,己烷显然是最佳溶剂,其二聚化效率略高于其他烷烃溶剂。
通过比较各种共轭二烯的光敏二聚化反应,我们可以确定不同的电子和结构因素对其反应性的影响。由于1,3-环己二烯具有较长的T1寿命和较活泼的1,4-二自由基三重态,因此其光二聚化反应最为活跃。因此,应该寻找光生物生产1,3-环己二烯的途径,尽管其缺点是它的非挥发性(b.p=80°C)使其无法在我们之前报道的两步光生物-光化学方法中用于喷气燃料碳氢化合物。
在非环共轭二烯中,异戊二烯二聚体的产率最高。重要的是,与1,3-环己二烯相比,异戊二烯具有足够的挥发性,可以从蓝藻细胞中逸出,从而促进其收获。然而,它在室温下仍然是液体,这使得它易于在光化学二聚化步骤中处理。这些优点使异戊二烯成为我们光生物-光化学两步合成航空燃料的理想的1,3-二烯。最小的共轭二烯,1,3-丁二烯,具有较低的光反应性,并且在环境温度(bp - 4°C)下为气体。其他线性共轭二烯的反应活性较低,是因为它们的甲基取代基数量较多,并且它们在T1态结构中的自由基特征被放置在内部碳上,这导致了更多的阻碍自由基并提供了超共轭稳定。事实上,我们的研究结果表明甲基取代模式影响了1,3-二烯的光敏二聚化,而三聚体寿命的巨大差异主导了对环1,3-二烯的影响。
光生物产生的二烯的捕获可能是在烷烃溶剂中。由于二烯的稀释降低了二聚化的产率,我们探索了提高光敏剂的负载,这提高了转化率,直到达到最佳负载,之后转化率下降。研究结果支持了我们通过小的1,3-二烯两步光生物-光化学生产喷气燃料碳氢化合物的进一步发展,特别关注异戊二烯作为最合适的二烯,因为它易于光生物获得,并且已知可以进行高效的光敏二聚化。
以下是电子补充材料的链接。
下载原文档:https://link.springer.com/content/pdf/10.1007/s43630-023-00418-0.pdf