随着全球COVID-19的第四个年头即将结束,美国疾病控制和预防中心(CDC)的数据显示,美国大多数感染、住院或死于SARS-CoV-2病毒的人都是老年人。该研究利用covid -19相关住院监测网络(COVID-NET)的数据进行,结果显示,与年轻年龄组相比,年龄≥65岁的成年人患covid -19相关住院和其他严重后果的风险增加。从Jan.-Aug。2023年,与covid -19相关的住院治疗中,近63%发生在65岁及以上的成年人中,其中许多人患有多种潜在疾病。相比之下,世界卫生组织(世卫组织)认为,在2020年至2021年期间,全球与covid -19相关的死亡人数中,80%以上发生在60岁或以上的人群中。
不幸的是,在美国住院的患者中,只有23.5%的人接种了推荐的COVID-19二价疫苗,只有58.6%的人接种了2020年底和2021年初推出的原始疫苗。在全球范围内,疫苗接种率似乎有所提高,全世界有超过55.5亿人接种了一剂COVID-19疫苗,约占世界人口的72.3%。然而,更深入的研究表明,不同国家的疫苗接种计划之间存在着明显的差距。
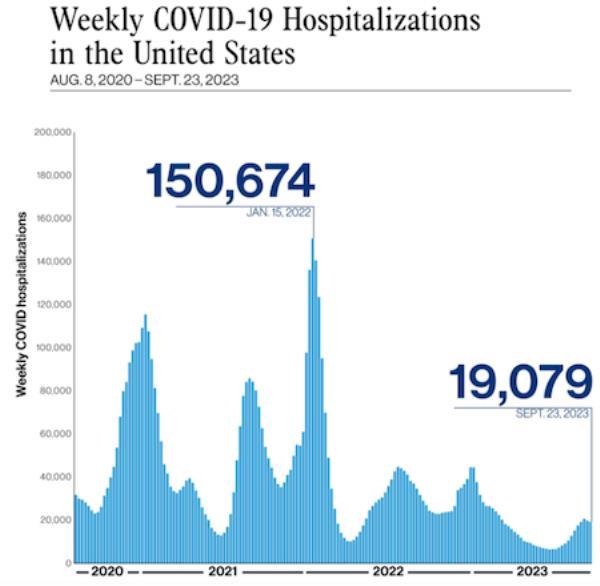
自2022年1月至9月,美国每周新冠肺炎病例数量大幅下降。2023. 来源:疾病预防控制中心
此外,虽然COVID-19最常在老年人和免疫功能低下人群中造成严重后果,但自2022年1月以来,呼吸道疾病(包括COVID-19、RSV和流感)已造成20多万人死亡,其中600人发生在19岁或以下的人群中。像流感一样,导致COVID-19的SARS-CoV-2很可能会继续存在。疫苗接种仍然是预防covid -19相关住院和死亡的最佳保护措施。它还可以减少长冠病毒的影响,长冠病毒可在急性感染期间或之后出现,并持续较长时间。
更新后的疫苗与以前的疫苗有何不同?谁应该接种疫苗?当前版本是否提供针对最近的COVID-19变体的保护?什么时候应该接种疫苗,其他季节性疫苗是否可以同时接种?
2022年秋季,可用的COVID-19疫苗是一种二价加强剂,针对BA.4和BA.5欧米克隆亚变体以及最初的SARS-CoV-2变体。在疫苗技术中,二价意味着在疫苗中引入两种不同的抗原,疫苗接种的目标是赋予对这两部分的保护。
辉瑞biontech和Moderna更新的COVID-19疫苗获批(9月中旬)。2023)由食品和药物管理局(FDA)和疾病预防控制中心推荐。更新后的疫苗再次是单价疫苗,旨在保护人们免受欧米克隆XBB.1.5亚型的侵害。虽然这种特定的变异目前仅占美国所有病例的3%左右,但目前流行的主要变异与它密切相关。换句话说,目前的COVID-19病毒非常接近疫苗版本,它将保护我们。
在mRNA疫苗开发之前,许多疫苗都是用一种微生物来挑战免疫系统,这些微生物要么是整个病原体,要么是某些关键成分。这意味着,在过去,世界依赖于使用弱化或灭活的病毒来制造疫苗,将其注射到鸡蛋(流感)、人类或其他宿主细胞中。这是一个漫长的过程,而且通常在疫苗可用的时候,传播的病毒已经发生了基因变化,使疫苗的效果降低。
mRNA疫苗完全颠覆了疫苗的制造。mRNA疫苗的工作方式不同,因为现在它们提供了一种人类细胞可以翻译成蛋白质的遗传密码(核酸语言)。因此,疫苗中的mRNA被用来促使宿主细胞产生病毒蛋白,在未来暴露/感染特定病原体时刺激免疫反应——通常是通过帮助用抗体中和病毒。此外,现有的COVID-19疫苗提供了有弹性的细胞介导免疫反应。
mRNA疫苗的惊人力量在于,生产它们所需的周转时间可以实时挽救生命。换句话说,疫苗制造商可以简单地调整当前流行的COVID-19变体(或流感等其他病毒)中发现的核酸代码,以包含从病毒外表面突出的“刺突”蛋白的代码,并在几周到一个月内,我们的身体可以免疫,最终复制当前变体的刺突蛋白,免疫系统随后学会识别。

虽然mRNA疫苗和传统
虽然两种疫苗的生产方式不同,但都旨在促进特异性和保护性免疫反应
宿主的鼻塞。来源:疾病预防控制中心
这些更新后的疫苗首次被批准适用于6个月及以上的所有人。Novavax COVID-19疫苗也于2023年10月初被批准用于12岁及以上的个体。美国疾病控制与预防中心的一项分析表明,制造一种普遍推荐的疫苗可以在未来两年内防止美国40万人住院治疗和4万人死亡。
简短的回答是肯定的,当前版本将会有保护。在2023年9月底,Omicron亚变体EG.5约占病例的29%(使其成为当时主要流行的SARS-CoV-2菌株),FL 1.51(另一个XBB后代)占病例的近14%。值得注意的是,目前疫苗中发现的XBB版本类似于EG.5,这将有助于提供保护。此外,根据疾病预防控制中心的说法,2023年8月出现的最新变种BA.2.86也应该被新的COVID-19疫苗所覆盖。
重要的是,包括SARS、RSV和流感在内的RNA病毒使生产长效疫苗变得非常困难,因为这些病毒在不断进化。换句话说,SARS-CoV-2在分子水平上是一个移动的目标。与流感疫苗和其他疫苗一样,这些新版本的COVID-19疫苗不能预防所有的COVID-19感染,但除非病毒发生重大的遗传转变,就像我们在2021年冬天从Delta到Omicron看到的那样,目前的COVID-19疫苗将提供部分到完全的保护,免受流行变体的影响。
此外,这些新版本的疫苗预计将对预防COVID-19感染导致的严重疾病、住院和死亡产生直接影响,而且这种疫苗的发布恰逢北半球的冬季,此时呼吸道感染、住院和死亡率往往会上升。
According to the CDC and WHO, the new COVID-19 vaccine should be taken in the fall, around the Sept.-Oct. timeframe (Northern Hemisphere) for best protection in the winter season. There may be a need for some individuals to receive the vaccine sooner (e.g., immunocompromised).
The COVID-19 vaccine is safe to receive at the same time as your annual influenza (e.g., flu) vaccine. The new respiratory syncytial virus (RSV) vaccine may be administered at the same time as well.
The CDC states that individuals who recently had a COVID-19 infection may wait up to 3 months before being vaccinated. And although experts collectively agree that people should wait until symptoms of an active COVID-19 infection resolve before getting vaccinated, there may be pros and cons to waiting for natural immunity to wane (~3 months) before boosting. On one hand, getting boosted before the 3 months have passed may produce higher levels of SARS-CoV-2 antibodies than what would be produced from COVID-19 infection alone, a factor that could make this a more desirable option, especially for those with high risk of SARS-CoV-2 exposure. However, waiting 3 months for natural immunity to wane, may generate a more robust antibody response upon boosting, which may be desirable for those who have a lower risk of day-to-day exposure.
In any case, it is important to stay up to date on vaccination, as people who do not get vaccinated after recovery from COVID-19 infection are more likely to get COVID-19 again than those who get vaccinated after their recovery.
Interested in learning more about COVID-19 variants, vaccines, policy and general FAQs? Check out our resource page!
Browse COVID-19 Resources /Public Release. This material from the originating organization/author(s) might be of the point-in-time nature, and edited for clarity, style and length. Mirage.News does not take institutio
nal positions or sides, and all views, positions, and co
nclusions expressed herein are solely those of the author(s).View in full here.
资讯来源:http://ansheng.wetsq.com/news/show-265745.html



